Электртерістілік. Коваленттік байланыс. Иондық байланыс. Металдық байланыс. (Химия, 10 сынып, I тоқсан)
Пән: Химия
Ұзақ мерзімді жоспар бөлімі: Атом құрылысы.
Сабақ тақырыбы: Электртерістілік. Коваленттік байланыс. Иондық байланыс. Металдық байланыс.
Осы сабақта қол жеткізілетін оқу мақсаттары (оқу бағдарламасына сілтеме): - атомның сыртқы аяқталған қабаты қандай жолмен түзілетінін анықтау;
- атомдар немесе иондардың электронды қосып алу немесе беріп жіберу салдарын түсіну;
- электртерістілік ұғымын білу;
- ковалентті байланыстың түзілу механизмін түсіндіру;
-иондық байланыстың түзілу механизмін түсіндіру;
Сабақ мақсаттары: Оқушылар жасай алады:
- «нүктелер мен айқыштар» диаграммасын сала білу
- коваленттік байланысты түсіну
- иондық тордың, молекулалық макромолекулалық және металл құрылысының қасиетін түсіну.
Өткен сабақ бойынша сұрақтар қойылады.
Оқушылар алгоритмді қолдана отырып, көрсетілген элементтер атомдарынан қалыптасқан химиялық байланыстың түзілу сызбасын құрастыру қажет. Ол үшін оқушыларға кесте беріледі. Кестенің бірінші бағанасында 5 тармақтан тұратын иондық байланыстың қалыптасу алгоритмі:
1. Металл атомының сыртқы энергетикалық деңгейінің электрондық
формуласын жазу.
2. Металл атомынан қалыптасатын ионның зарядын анықтау.
3. Бейметалл атомының сыртқы энергетикалық деңгейінің электрондық
формуласын жазу.
4. Бейметалл атомынан қалыптасатын ионның зарядын анықтау.
5. Иондық байланыстың қалыптасу сызбасын жазу, қажет болса
коэффициенттерін қою.
A) кальций және фтор
B) натрий және оттегі
Тапсырма 10 минутқа арналған.
Оқушыларға неліктен ас тұзының ерітіндісі тоқты өткізетіндігін, ал неліктен тұздың қатты түрі тоқты өткізбейтіндігін сұраңыз.
Неліктен дистелденген су тоқ көзін өткізбейді? Ал неліктен техникалық су тоқ көзін өткізеді?
Қалай ойлайсыздар?
Кристалдық тор дегеніміз не? Оқушылар өздері ізденеді.
«нүктелер мен айқыштар» диаграммасы идеясын енгізу
Dot-and-cross diagrams are used to show the electronic configurations of elements and ions. The electronic of one element in the compound are shown by dots, those of the second element by crosses.
Covalent molecules:
A covalent bond is formed by the sharing of electrons between non- metals to achieve state electronic configuration.
There are two types of covalent moelcules. Simple molecules, and giant molecules. In this section, we will be looking at simple molecules.
Оқушыларға видеоролик көрсету.
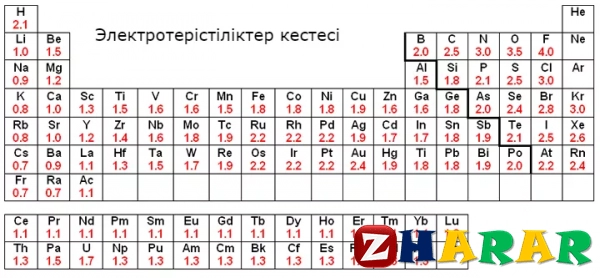
Оқушыларға электртерістілікті түсіндіру:
Electronegativity, symbol χ, is a chemical property that describes the tendency of an atom or a functional group to attract electrons (or electron density) towards itself. An atom's electronegativity is affected by both its atomic number and the distance at which its valence electrons reside from the charged nucleus. The higher the associated electronegativity number, the more an element or compound attracts electrons towards
оқушылар (f) оларды біртіңдеп күрделендіре отырып, өз мысалдарын келтіреді
Draw dot-and- cross diagrams for the following:
a. KF
b. Na2O
c. MgO
d. CaCI2
Жаңа сабақ тақырыбы, мақсаттары презентация арқылы көрсетіледі.
Электрондарды біріктіруге ауысыңыз: оның сыртқы қабаттың тұрақтылығына қалай әсер ететінін, бірақ заряд бөліміне әсер етпейтіндігін түсіндіріңіз.
Коваленттік байланысты көрсету үшін «нүктелер мен айқыштар» диаграммасын қалай пайдалану керектігін түсіндіру
Оқушылар сабақ бойына кездескен жаңа терминдерді сөздік дәптерге жазып отырады.
Оқушыларға ақ шағын тақташалар беріледі. Оқушылар назарына кезек-кезек 4 химиялық қосылыстың формулалары келтіріледі. Оқушылар жауабын «нүктелер мен айқыштар» диаграммасы түрінде ұсыну қажет.
Осы тапсырманы орындау барысында мұғалім келтірілген барлық қосылыстар үшін «нүктелер мен айқыштар» диаграммасын дұрыс құрастыра алған оқушыларды және де тапсырманы тек жарым-жартылай орындаған оқушыларды белгілейді.
Тапсырма 10 минутқа арналған.
Тапсырма тікелей сабақ барысында бағаланады. Нәтижелерін мұғалім кесте түрінде, оқушылардың аты-жөніне қарама-қарсы әр қосылыс бойынша тапсырманы кім тез, ал кім кеш жасағанын, кім тапсырманы орындай алмағанын белгілейді.
Оқыту барысының соңында мұғалім әрі қарай оқушылардың жеке даму траекториясын құрастыру үшін қойылған мақсатқа жете алмаған оқушыларды анықтайды.
Иондық кристалдар
Иондық кристалдар аттас зарядталған иондардың электростатикалық әсерінің нәтижесінде түзіледі. Кристалдың иондық моделі әрбір ионның максималды жағдайда аттас зарядталған иондармен қоршалуы нәтижесінде түзіледі.
АВ құрамды кристалдар үшін иондық радиустың қатынасы иондардың координациялық санын құрайды. Иондық кристалдық торды тұздар және сілтілер түзеді.......
Ұзақ мерзімді жоспар бөлімі: Атом құрылысы.
Сабақ тақырыбы: Электртерістілік. Коваленттік байланыс. Иондық байланыс. Металдық байланыс.
Осы сабақта қол жеткізілетін оқу мақсаттары (оқу бағдарламасына сілтеме): - атомның сыртқы аяқталған қабаты қандай жолмен түзілетінін анықтау;
- атомдар немесе иондардың электронды қосып алу немесе беріп жіберу салдарын түсіну;
- электртерістілік ұғымын білу;
- ковалентті байланыстың түзілу механизмін түсіндіру;
-иондық байланыстың түзілу механизмін түсіндіру;
Сабақ мақсаттары: Оқушылар жасай алады:
- «нүктелер мен айқыштар» диаграммасын сала білу
- коваленттік байланысты түсіну
- иондық тордың, молекулалық макромолекулалық және металл құрылысының қасиетін түсіну.
Өткен сабақ бойынша сұрақтар қойылады.
Оқушылар алгоритмді қолдана отырып, көрсетілген элементтер атомдарынан қалыптасқан химиялық байланыстың түзілу сызбасын құрастыру қажет. Ол үшін оқушыларға кесте беріледі. Кестенің бірінші бағанасында 5 тармақтан тұратын иондық байланыстың қалыптасу алгоритмі:
1. Металл атомының сыртқы энергетикалық деңгейінің электрондық
формуласын жазу.
2. Металл атомынан қалыптасатын ионның зарядын анықтау.
3. Бейметалл атомының сыртқы энергетикалық деңгейінің электрондық
формуласын жазу.
4. Бейметалл атомынан қалыптасатын ионның зарядын анықтау.
5. Иондық байланыстың қалыптасу сызбасын жазу, қажет болса
коэффициенттерін қою.
A) кальций және фтор
B) натрий және оттегі
Тапсырма 10 минутқа арналған.
Оқушыларға неліктен ас тұзының ерітіндісі тоқты өткізетіндігін, ал неліктен тұздың қатты түрі тоқты өткізбейтіндігін сұраңыз.
Неліктен дистелденген су тоқ көзін өткізбейді? Ал неліктен техникалық су тоқ көзін өткізеді?
Қалай ойлайсыздар?
Кристалдық тор дегеніміз не? Оқушылар өздері ізденеді.
«нүктелер мен айқыштар» диаграммасы идеясын енгізу
Dot-and-cross diagrams are used to show the electronic configurations of elements and ions. The electronic of one element in the compound are shown by dots, those of the second element by crosses.
Covalent molecules:
A covalent bond is formed by the sharing of electrons between non- metals to achieve state electronic configuration.
There are two types of covalent moelcules. Simple molecules, and giant molecules. In this section, we will be looking at simple molecules.
Оқушыларға видеоролик көрсету.
Оқушыларға электртерістілікті түсіндіру:
Electronegativity, symbol χ, is a chemical property that describes the tendency of an atom or a functional group to attract electrons (or electron density) towards itself. An atom's electronegativity is affected by both its atomic number and the distance at which its valence electrons reside from the charged nucleus. The higher the associated electronegativity number, the more an element or compound attracts electrons towards
оқушылар (f) оларды біртіңдеп күрделендіре отырып, өз мысалдарын келтіреді
Draw dot-and- cross diagrams for the following:
a. KF
b. Na2O
c. MgO
d. CaCI2
Жаңа сабақ тақырыбы, мақсаттары презентация арқылы көрсетіледі.
Электрондарды біріктіруге ауысыңыз: оның сыртқы қабаттың тұрақтылығына қалай әсер ететінін, бірақ заряд бөліміне әсер етпейтіндігін түсіндіріңіз.
Коваленттік байланысты көрсету үшін «нүктелер мен айқыштар» диаграммасын қалай пайдалану керектігін түсіндіру
Оқушылар сабақ бойына кездескен жаңа терминдерді сөздік дәптерге жазып отырады.
Оқушыларға ақ шағын тақташалар беріледі. Оқушылар назарына кезек-кезек 4 химиялық қосылыстың формулалары келтіріледі. Оқушылар жауабын «нүктелер мен айқыштар» диаграммасы түрінде ұсыну қажет.
Осы тапсырманы орындау барысында мұғалім келтірілген барлық қосылыстар үшін «нүктелер мен айқыштар» диаграммасын дұрыс құрастыра алған оқушыларды және де тапсырманы тек жарым-жартылай орындаған оқушыларды белгілейді.
Тапсырма 10 минутқа арналған.
Тапсырма тікелей сабақ барысында бағаланады. Нәтижелерін мұғалім кесте түрінде, оқушылардың аты-жөніне қарама-қарсы әр қосылыс бойынша тапсырманы кім тез, ал кім кеш жасағанын, кім тапсырманы орындай алмағанын белгілейді.
Оқыту барысының соңында мұғалім әрі қарай оқушылардың жеке даму траекториясын құрастыру үшін қойылған мақсатқа жете алмаған оқушыларды анықтайды.
Иондық кристалдар
Иондық кристалдар аттас зарядталған иондардың электростатикалық әсерінің нәтижесінде түзіледі. Кристалдың иондық моделі әрбір ионның максималды жағдайда аттас зарядталған иондармен қоршалуы нәтижесінде түзіледі.
АВ құрамды кристалдар үшін иондық радиустың қатынасы иондардың координациялық санын құрайды. Иондық кристалдық торды тұздар және сілтілер түзеді.......
Толық нұсқасын 30 секундтан кейін жүктей аласыз!!!
Әлеуметтік желілерде бөлісіңіз:
Facebook | VK | WhatsApp | Telegram | Twitter
Қарап көріңіз 👇
Пайдалы сілтемелер:
» Туған күнге 99 тілектер жинағы: өз сөзімен, қысқаша, қарапайым туған күнге тілек
» Абай Құнанбаев барлық өлеңдер жинағын жүктеу, оқу
» Дастархан батасы: дастарханға бата беру, ас қайыру
Соңғы жаңалықтар:
» Су тасқынынан зардап шеккендерге қосымша тағы 553 мың теңге төленеді
» Елімізде TikTok желісі бұғатталуы мүмкін бе?
» Елімізде су тасқынынан зардап шеккендердің қандай мүліктеріне өтемақы төленеді?

